저작자표시-비영리-변경금지 2.0 대한민국 이용자는 아래의 조건을 따르는 경우에 한하여 자유롭게 l 이 저작물을 복제, 배포, 전송, 전시, 공연 및 방송할 수 있습니다. 다음과 같은 조건을 따라야 합니다: l 귀하는, 이 저작물의 재이용이나 배포의 경우, 이 저작물에 적용된 이용허락조건 을 명확하게 나타내어야 합니다. l 저작권자로부터 별도의 허가를 받으면 이러한 조건들은 적용되지 않습니다. 저작권법에 따른 이용자의 권리는 위의 내용에 의하여 영향을 받지 않습니다. 이것은 이용허락규약(Legal Code)을 이해하기 쉽게 요약한 것입니다. Disclaimer 저작자표시. 귀하는 원저작자를 표시하여야 합니다. 비영리. 귀하는 이 저작물을 영리 목적으로 이용할 수 없습니다. 변경금지. 귀하는 이 저작물을 개작, 변형 또는 가공할 수 없습니다.
이학 박사학위 논문
DUR시스템에 대한 중복 예외처방
사유 분석
Analyzing alert overrides reasons in the Drug Utilization Review system
아주 대학교 대학원
의학과 / 의학전공
DUR 시스템에 대한 중복 예외처방
사유 분석
Analyzing alert overrides reasons in the Drug Utilization Review system
지도교수 박 래웅
이 논문을 이학박사학위 논문으로 제출함
2016년 2월
아주 대학교 대학원
의학과 / 의학전공
장 철
장 철의 이학 박사학위 논문을 인준함
심사위원장 박 범 인
심 사 위 원 박 래 웅 인
심 사 위 원 신 승 수 인
심 사 위 원 이 영 호 인
심 사 위 원 정 은 영 인
아 주 대 학 교 대 학 원
2015년 12월 18일
감사의 글
불혹의 나이에 설렘과 두려움을 안고 대학원 입학 할 때가 엊그제 같은데 이 젠 10여년의 세월이 흘러 드디어 박사학위 논문을 최종 마무리하는 와중에 지 나온 세월들이 새삼 병풍처럼 스쳐갑니다. 수많은 어려움과 노력하는 과정에서 학문의 길 뿐 아니라 인격 수양에 중요 한 시간들이었고, 무엇보다 박사학위 논문이란 하나의 큰 결과물을 얻기까지 지도 편달해 주신 박 래웅 교수님께 글로 표현 할 수 없을 정도로 깊은 감사와 경외를 표합니다. 앞으로 교수님 은혜에 조금이나마 보답이 되도록 더욱 더 열심히 노력하는 자세로 임하겠습니다. 또한 너무 바쁘신 와중에도 냉철한 눈으로 데이터 분석과 논문 주제 및 방향 설정에 크나 큰 도움을 주신 유 기봉 교수님께 깊은 감사를 드리며, 선행 연구 자로서 논문 검토와 자료를 아낌없이 주신 안 은경 교수님, 김 우재 교수님, 그리고 박 만영 박사에게도 감사의 글을 올립니다. 앞으로 하고자 하시는 분야에서 최고가 되실 수 있도록 기원하겠고, 제 자신 또한 밀알이 되도록 하겠습니다. 또한 바쁘신 와중 이 논문을 열과 성의로 심사해 주시고 많은 지적을 해 주신 박 범 교수님, 신 승수 교수님, 이 영호 교수님, 그리고 정 은영 박사님께 감사 의 글 올립니다. 더불어 직, 간접적으로 많은 도움을 주신 회사 동료와 대학원 동료들, 그리고 도움주신 친구들에게 감사드립니다.10 년 전 대학원에 입학할 시부터 지금까지 묵묵히 믿어주고, 물심양면으로 도움을 주신 사랑하는 아내 이 경희, 당신이 내 생에 최고의 선물이라 생각 하며, 깊이 감사드리고 고마움을 전합니다. 의학도의 어려운 길을 선택하여 불철주야 열심히 공부하면서 논문 완성에 기 여해 준 자랑스러운 아들 지우, 고3 수험생으로 늦게까지 열공 하면서 같이 밤을 새워주고 좋은 결과로 새내기 대학생이 되는 사랑스런 딸 예슬, 너무 너 무 감사하고, 이제는 우리 가족들의 은혜에 보답할 수 있도록 최선의 노력을 다 하는 아버지와 가장이 될 것을 새삼 다짐해 봅니다. 마지막으로 불의의 사고로 병원에서 재활 치료 중인 지현이와 이를 돌보며 늘 기도하시는 누나와 매형에게 힘과 용기를 주시고, 빠른 완쾌로 가족들 모두 행복하시길 기도드리며, 이 논문을 바칩니다. 2015년 마지막 날에! 장 철 올림.
DUR시스템에 대한 중복예외처방 사유 분석
우리나라는 모든 의료기관에서 단일체계의 의약품사용평가시스템을 사용하고 있다. 의약품사용평가시스템의 효율적 운영을 위해서는 발생되는 경고 및 그 중에서 무시되는 경고에 대한 지속적인 모니터링이 필요하다. 본 연구에서는 일개 병원의 의약품사용평가시스템에서 발생하는 중복예외처방경고에 대하여 경고를 무시하고 처방을 진행하는 경우에 있어서, 중복예외처방경고에 대한 예 외처방 사유코드 및 사유내용현황을 조사함으로써, 기존의 중복예외처방 사유 코드의 개선 가능성을 모색하고자 한다. 경기도 소재 1개 대학병원에서 2012년 4월부터 2013년 1월 15일까지 내원 한 환자에게 수행한 약 처방 중에 발생한 모든 중복 예외처방 경고건수를 연구 대상으로 하여 기술 분석을 수행하였다. 해당 기간 중 예외처방 사유코드가 입 력된 건은 외래 처방에서 7,772건이었고, 외래, 입원, 응급 및 기타의 과에서 예외처방 사유코드가 아닌 자유진술문으로 입력된 예외처방사유내용 건수는 총 89,686건이었다. 이들 예외처방사유내용을 분류하기 위하여 연구자간의 합의에 의하여 13개의 분류그룹을 선정하고, 3명의 연구자가 이들 89,686건의 예외처 방사유내용을 수작업으로 분류하였다. 이들 13개의 분류그룹과 기존 건강보험심사평가원의 11개 예외처방 사유코드 를 분류 및 비교하여 다음과 같은 주요 결과를 도출하였다. 첫째로 외래, 입원, 응급 전체에 대한 예외처방사유내용을 분석한 결과, 가장 높은 비율을 차지한 것은 처방 약이 같은 시간대 투약이 아닌 경우가 31.6% (28,306건)로 나타났으며, 이어서 질병이나 증상을 표기한 경우가 22.2%(19,9 09건)를 차지하였다. 둘째, 예외처방사유내용이 입력된 건에서 해당 처방이 발생될 당시의 진단명 빈도를 국제표준코드인 ICD-10코드에 따라 분석한 결과, 가장 높은 비율을 차지한 진단코드는 M코드(근골격계)로서 23.6% (21,183건)이었으며, J코드(호흡 기계) 11.5%, K코드(소화기계) 10.1% 순이었다. 셋째, 예외처방사유내용이 입력된 건에서 해당 처방이 발생될 당시에 문제가 된 약품의 빈도를 국제의약품분류코드인 ATC 코드를 이용하여 분석한 결과, 예외처방사유내용 중 가장 높은 비율을 차지한 ATC코드는 M(근골격계)으로서 전체의 절반이 넘는 56.8%(50,950건)를 차지하였고, 이어서 C(심혈관계) 10. 8%(9,651건), L(항종양제 및 면역조절제) 9.5%(8,523건), 그리고 N(신경계)가 7.1%(6,330건) 순이었다. 본 연구를 통해서 외래, 입원, 응급 등 총 환자들 중 예외처방사유내용에 대 한 자유진술문으로 입력된 모든 예외처방사유내용을 분석하여 기존 11개 코드 로의 변환 가능성을 모색하였고, 사용자가 자유진술문으로 입력하지 않고 손쉽 게 코드를 선택하여 입력할 수 있도록 새롭게 6개의 분류코드를 제안하였다. 하지만, 본 연구는 다음과 같은 제한점이 있다. 1개 대학병원의 약 10개월간 처방자료만 사용하였기 때문에 지역적, 시간적 및 질병 중증도에 따른 선택편 견의 가능성이 있다. 또한, 예외처방사유내용을 연구자가 임의로 설정한 13 개 의 코드로 매핑 하는 과정에서, 연구자들의 주관성이 작용하여 분류오류가 있 었을 가능성이 있다. 그럼에도 불구하고, 자유진술문으로 입력된 방대한 양의 예외처방사유를 직접 분석하고 이를 기존의 예외처방코드와 통합한 점은 본 연 구의 장점으로 본다.
핵심어: 의약품사용평가시스템, Drug Utilization Review, 중복예외처방코드, Alert override codes, 약물상호작용, Drug-Drug Interaction,
차 례
Ⅰ. 서 론 ··· 1 A. 연구의 배경 및 필요성 ··· 1 B. 연구의 목적 ··· 8 C. 이론적 배경 및 선행연구 ··· 9 1. 의약품사용평가시스템 ··· 9 2. 선행연구 ··· 11 Ⅱ. 연구방법 ··· 17 A. 연구대상 자료 분석 ··· 17 B. 연구대상 비교 코드 ··· 22 III. 연구결과 ··· 24 A. 외래환자의 중복예외처방코드(HIRA) 분석결과 ··· 24 1. 월별 분석 ··· 24 2. 연령별 분석 ··· 25 3. DDI의 중복예외처방 코드(HIRA) 빈도분석 ··· 26 4. ATC코드 빈도분석 ··· 27 5. ICD 코드 빈도분석 ··· 29 6. ATC 코드와 중복예외처방(HIRA)코드의 교차분석 ··· 31 7. ICD코드와 중복예외처방코드(HIRA)의 교차분석 ··· 32 B.외래, 입원, 응급, 기타의 중복예외처방사유(Free-text)분석 결과 ··· 34 1. 전체 중복예외처방사유내용(13개 분류) 분석 ··· 34 2. 연령과 중복예외처방사유(Free-text)분석 ··· 35 3. ICD코드와 중복예외처방사유(Free-text)분석 ··· 37 4. ATC코드와 중복예외처방사유(Free-text)분석 ··· 42 C. 새로운 DDIs 중복예외처방코드 제시 ··· 45IV. 고찰 ··· 49 A. DUR 시스템의 DDIs 중복예외처방 사유 분석 ··· 49 B. 새로운 DDIs 중복예외처방코드 제안 및 제언 ··· 52 V. 결 론 ··· 58 참고문헌 ··· 62 부 록 ··· 69 ABSTRACT ··· 87
표 차례
Table 1. Rationale behind the Drug Epidemiological Studies and Drug
Surveillance after Approval of Sales ··· 6
Table 2. Post-Sale Drug Monitoring System ··· 7
Table 3. The significance ratings of drug interactions ··· 14
Table 4. Factors related to drug–drug interaction ··· 15
Table 5. Examples of drug-drug interactions in oncology ··· 16
Table 6. Subject groups ··· 18
Table 7. Fourteen Anatomical Main Groups of the First Level of the ATC Codes ··· 23
Table 8. Age Distribution ··· 25
Table 9. Frequency of Overlapping Prescription Codes Among the 7,772 Outpatient Cases (Grounds for the Report) ··· 26
Table 10. Frequency of ATC Codes among the 7,772 Outpatient Cases with Overlapping Prescription Codes (Grounds for the Report) 28 Table 11. Frequency of ICD codes among the 7,772 Outpatient Cases with Overlapping Prescription Codes ··· 30
Table 12. Cross Tabulation of ATC Codes and Overlapping Prescription Codes B and P ··· 32
Table 13. Cross Tabulation of ICD Codes and Overlapping Prescription Codes B and P ··· 33
Table 14. Classification of Alert Override Reasons ··· 34
Table 15. Cross Tabulation of Age Groups and Alert Override Reasons ··· 36
Table 16. Cross Tabulation of ICD Codes and Alert Override Reasons ··· 38
Table 17. Cross Tabulation of ATC Codes and Alert Override Reasons ··· 43 Table 18. Frequency of Overlapping Prescription Codes of the Health Insurance Review and Assessment Service ··· 45 Table 19. Frequencies of Override Reasons in Free Text ··· 46 Table 20. Frequency of Alert Override Reasons Using New Classification
System ··· 48 Supplement 1. Frequency of ATC Codes in 7,772 Outpatient Cases with Therapeutic Duplication ··· 69 Supplement 2. Frequency of ICD Codes in 7,772 Outpatient Cases of
그림 차례
Figure 1. Number of Domestic Drug-Related Adverse Events Reported
per Year ··· 4
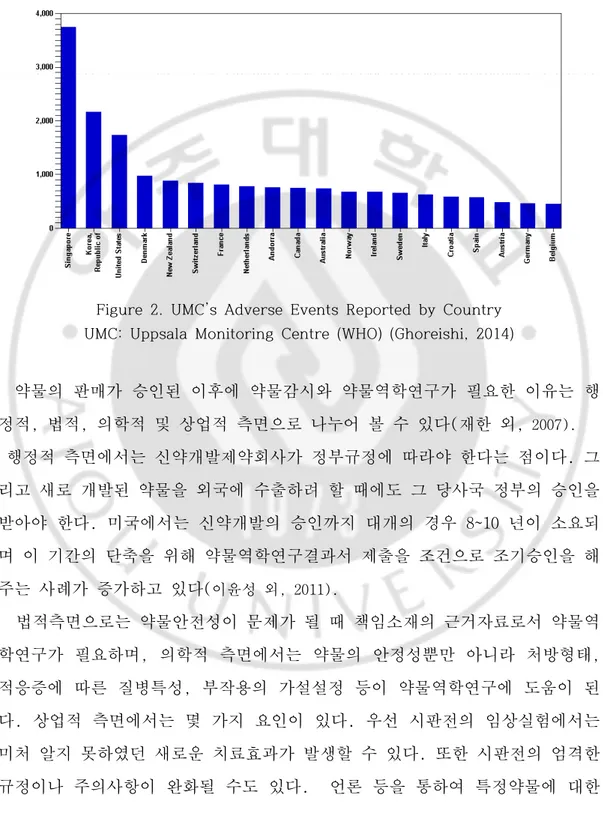
Figure 2. UMC’s Adverse Events Reported by Country ··· 5
Figure 3. Work flow for Drug Utilization Review (DUR) ··· 10
Figure 4. Study framework ··· 19
Figure 5. Data selection process ··· 21
Figure 6. Age Distribution ··· 25
Figure 7. Analysis on Frequency of Duplicate Prescription Private Code ··· 27
Ⅰ. 서 론
A. 연구의 배경 및 필요성
역사적으로 약물요법이 질병의 주요치료수단이 된 것은 오래되지 않았다. 1900년대 초까지도 약물들은 과학적인 검증절차 없이도 시중에 판매되었다(박 윤재, 2014). 몇 가지 대규모 약물 사건들은 의약품에 대한 검증의 필요성이 제 기되었고, 그 과정이 법으로 제정되는 계기가 된다. 예를 들어 1937년 설파닐 아미드 (sulfanilamide) 투약으로 인하여 107명이 신부전으로 사망하였고(Mitc hell et al., 1940), 이를 계기로 1938년에는 식품의약품 화장품 법(Food, Dru g, and Cosmetic Act)이 제정되었다(U.S. FDA, 1937). 이후로 약물의 시판을 위 해선 제약회사에서는 임상 독성 실험을 해야 하고, 식품의약품안전국(FDA)에 신고가 의무화 된다. 1957년에 독일에서 탈리도마이드가 단기수면제로 허가가 되었는데, 입덧에 효과가 있어서 많은 임산부들이 복용하게 된다. 예상하지 못 하게 이 약을 복용한 임산부들에서 1만 명의 사지결손증 환자가 태어나는 사건 이 발생하였다(Ghoreishi, 2014). 이를 계기로 미국에서는 1962년에 키포버-해 리스 수정법안을 통과시켜 시판 전에 약물안정성확인을 더욱 엄격하게 규정 하 였고, 신약임상시험계획승인(Investigational New Drug Application, INDA)과 정부 신약 허가신청 (New Drug Application, NDA)로 귀결 되었다(http://www.dr ugstudy.md/resource9.html, 2015). 또한 세계보건기구에서는 1968년부터 국제 약 물모니터링 프로그램을 구성한 후 세계 각국에서 약물유해사례에 대한 정보를 수집하게 된다. 그리고 1989년에는 국제 약물역학회 (International Society f or Pharmacoepidemiology, ISPE)가 구성되어 매년 북미와 유럽에서 한차례씩 국제학술대회를 개최하고 있다. (https://www.pharmacoepi.org/about/history.cfm, 2015). 미국에서는 매년 수백만 명이 약물유해반응으로 입원하고 있으며, 10만 명이약물유해반응으로 병원에서 사망하고 있다(Lee et al., 2007).
미국의 Institute of Medicine (IOM)의 보고에 의하면, 전체 의료과오 중 약 물부작용이 차지하는 비율은 20%이며, 입원하는 환자 중 44,000~98,000명이 매 년 약물과 관련된 의료사고 (Medical error)로 사망한다(Kohn et al., 2000). 그리고 미국보건후생성본부의 보고에 의하면 의료사고 사망자들 중 약 7천명이 약물관련 부작용에 의한 것 이었다(Chae et al., 2013;범희승 외, 2002). 1990년 부터 2005년까지 보고된 문헌들을 분석한 결과에서도, 병원입원환자들 중에서 투약오류(medication errors) 그리고/또는 약물부작용사건 (adverse drug even ts)이 발생한 비율은 전체 약물처방 중 대략 5.7%로 나타난 바 있다(Krahenbuhl -Melcher et al., 2007).
개별 병원(1차병원)에서의 약물 부작용에 대한 보고도 진행되어 왔는데, 예를 들어 미국 보스턴의 Brigham and Women's 병원에서는 입원환자 100명당 5.5명 이 약물 부작용을 경험하였고, 이로 인해 입원까지 하였던 것은 1천 명당 3.4 건, 그리고 생명에 지장을 줄 정로로 심각하였던 상황은 23%였다(Honigman et al., 2001). 이러한 상황은 약물유해반응으로 사망하는 손실은 국민 보건 상 총 기사고, 음주, 흡연을 모두 합한 것보다 더 큰 것이다. 이것은 약물유해 반응 해결에 소요되는 비용에서 더욱 분명해진다. 즉, 약물유해반응과 관련된 비용 은 당뇨나 심장병 치료에 드는 총 의료비용 보다 많은 연간 1,360억 달러에 이 른다. 이러한 상황은 미국만이 아니라 전 세계적인 문제로서, 의료영역을 넘어 서서 사회적인 문제로 부각되고 있는 것이다. 주목할 만한 사실들은 전체 약물 부작용의 38%는 충분히 예방이 가능한 경우로 판단되었다는 점이다. 따라서 약물부작용의 발생을 방지하려는 노력이 다각적이며, 지속적으로 이루 어져 왔는데, 그 방법들은 자발적인 보고(Volunteer reporting), 의무기록조사 (Chart Review), 약물부작용감시시스템(Adverse Drug Event)으로 크게 세 가지 로 나뉠 수 있다. Jha et al.(1998)의 연구에 의하면 이들 세 가지 방법 중 약 물부작용감시시스템으로 인한 발견수치가 가장 많았다. 그리고 약물부작용의 발생을 방지하려는 노력으로 의약품사용평가시스템(Drug Utilization Review,
DUR)이 포함된다. 의약품사용평가 시스템 (DUR)제도는 부적절한 약물의 처방과 조제를 방지하여 약물 부작용을 예방하고 문제의약품의 사용을 줄일 수 있도록 지원하는 시스템 으로서 약물 부작용을 예방할 수 있는 효과적인 방법으로 알려져 있다(Lyles et al., 2001). 미국에서는 이미 1990년부터 본 제도를 실시하고 있으며, 우리 나라는 2010년 12월 "의약품 처방, 조제지원서비스(DUR)"를 구축, 이후 전국 요양기관으로 확대 실시하였다. 우리나라의 DUR 시스템은 크게 처방전내 점검 과 처방전 외 점검의 두 가지로 나뉠 수 있으며, 여기서 제공되는 정보내용에 는 병용금기, 연령금기, 임부금기 의약품, 저함량 배수처방 조제의약품, 안전 성관련 급여중지의약품, 동일 투여경로의 동일성분 중복처방 등이 포함된다. 처방과정에서 병용금기, 연령금기, 임부금기, 동일성분 중복처방 의약품 등으 로 인하여 팝업 경고창이 발생한 경우에는 그 사유를 기재한 후 처방 또는 조 제를 진행 할 수 있다(전하림 외, 2014 ). 한편, 약물감시는 다시 사전약물감시와 사후약물감시의 두 영역으로 나뉠 수 있다. 전통적으로 신약의 승인을 위해서는 8~10 여년이 필요하였으나, 최근 미 국에서는 신약의 승인기간단축을 위해서 약물역학연구결과를 제출하는 것을 조 건으로 조기승인을 해주는 비율이 증가하고 있다(이윤성 외, 2011). 이러한 상 황은 사후약물감시의 중요성을 더욱 증가시키는 원인이 된다. 사후 약물감시는 사전 약물감시에 비해 대규모의 다양한 인구집단을 대상으로 장기간의 관찰을 할 수 있다는 장점을 갖는다. 따라서 단기간에 제한된 연구 집단을 대상으로 진행되어 사전에 알 수 없었던 약물의 부작용에 대한 확인과정으로서 중요한 의미를 갖는다. 실제로 1980년 이후에 지금까지 수많은 약물들이 시판 후 심각한 약물유해반응이 밝혀지면서 퇴출된바 있다(Lake et al., 1990; Qureshi et al., 2011; Fung et al., 2001).
시판 전 임상실험 등의 과정을 통해 약물의 안전성이 사전에 검토되어 과거와 같이 대규모의 약물 부작용의 발생 가능성은 최소화되고 있다(Park, 2013). 하지만 시판허가를 위한 임상실험은 관찰기간이 제한되어 있을 뿐 만 아니라
연구 대상자의 수와 연구대상자의 범위가 제한된다는 한계점을 가지고 있다(이 진호, 2012). 또한 연구 대상 확보에 어려움이 있고 연구기간이 오래 걸리며 연 구비가 많이 들게 된다. 무엇보다 다양한 종류의 상황과 사람을 대상으로 한 것이 아니기 때문에 실제 현장에서 약물의 증상은 현실적으로 시판 전에 모두 예측하기 어렵다. 시판 후에는 남녀노소 많은 수의 환자들이 약물을 이용하게 되고, 장기간 복용하게 되는 경우도 빈번해진다. 따라서 시판 전 임상에서 발 견하지 못하였던 중대한 위해반응들이 나타날 가능성을 배제할 수 없는 것이 다. 단적인 예로 세계적으로 약물유해반응의 사례보고는 국가마다 차이가 나지 만 100만 명 당 핀란드의 500여건에서 상가포르의 2,800건까지 상당한 숫자에 이른다(그림 2). 이러한 약물유해문제는 해가 갈수록 다양한 약물이 개발되기 에 약물유해반응의 사례도 증가하게 된다. 예를 들어 연도별 국내 의약품 유해 사례보고 건수는 2003년의 199건에서 매년 증가하여 2006년에는 6,239건, 2009 년에는 27,000건, 2012년에는 92,615건,2013년에는 10월까지 총 140,000건이 되고 있다(그림 1).
Figure 1. Number of Domestic Drug-Related Adverse Events Reported per Year
Figure 2. UMC’s Adverse Events Reported by Country UMC: Uppsala Monitoring Centre (WHO) (Ghoreishi, 2014)
약물의 판매가 승인된 이후에 약물감시와 약물역학연구가 필요한 이유는 행 정적, 법적, 의학적 및 상업적 측면으로 나누어 볼 수 있다(재한 외, 2007). 행정적 측면에서는 신약개발제약회사가 정부규정에 따라야 한다는 점이다. 그 리고 새로 개발된 약물을 외국에 수출하려 할 때에도 그 당사국 정부의 승인을 받아야 한다. 미국에서는 신약개발의 승인까지 대개의 경우 8~10 년이 소요되 며 이 기간의 단축을 위해 약물역학연구결과서 제출을 조건으로 조기승인을 해 주는 사례가 증가하고 있다(이윤성 외, 2011). 법적측면으로는 약물안전성이 문제가 될 때 책임소재의 근거자료로서 약물역 학연구가 필요하며, 의학적 측면에서는 약물의 안정성뿐만 아니라 처방형태, 적응증에 따른 질병특성, 부작용의 가설설정 등이 약물역학연구에 도움이 된 다. 상업적 측면에서는 몇 가지 요인이 있다. 우선 시판전의 임상실험에서는 미처 알지 못하였던 새로운 치료효과가 발생할 수 있다. 또한 시판전의 엄격한 규정이나 주의사항이 완화될 수도 있다. 언론 등을 통하여 특정약물에 대한
유해보도가 나올 때 대응하기 위한 방법으로도 약물역학연구가 활용되어 해당 약물을 보호할 수 있다(박정규, 1998).
자료 : http://www.drugstudy.md/resource9.html.
Aspects Details
Administrative Government policies on sales; government policies in countries importing new drugs Legal Obtain evidence of liability for drug safety Medical
Maintain drug safety; identify prescription patterns; identification of the characteristics of diseases according to indicants; establishing hypotheses on side effects
Commercial
Discovery of new treatment effects; alleviation of strict regulations and precautions; response to news reports on harmfulness of certain drugs
Table 1. Rationale behind the Drug Epidemiological Studies and Drug Surveillance after Approval of Sales
자료 : http://www.drugstudy.md/resource9.html. System Details Voluntary reporting system for side effects Started in 1988
The number of reports increased during the 2000s after the Korea Food and Drug Administration mandated that pharmaceutical companies and pharmacies make reports at the time of sales approval.
Several university hospitals were designated as regional pharmacovigilance centers in 2006.
The Pharmacovigilance Corporation was founded in 2009, and the number of reports increased as the number of regional pharmacovigilance centers in South Korea increased to 20.
Re-exami nation system
Started in January 1995
For 6 years after the approval of new drugs, their safety and efficacy should be reported to the Korea Food and Drug Administration after administration to 3,000 patients in everyday clinical settings.
For drugs that are not completely new, reports should be made after the drug has been administered to 600 patients within 4 years.
Re-evalu ation system
Started in 1975
Collect and evaluate case reports and clinical studies published after the approval of sales.
Add newly discovered indicants and adverse effects to the label information.
Reorganize irrelevant results of pre-approval clinical studies from the label information.
B. 연구의 목적
우리나라는 한방분야를 제외하고는 모든 의료기관과 요양기관에서 단일체계 의 DUR시스템을 사용한다는 장점을 가지고 있으며, 시스템의 관리 여하에 따라 상당한 정보를 추출, 활용할 수 있는 가능성이 있다. 따라서 효과적인 DUR시스 템이 정착되기 위해서는 지속적인 모니터링과 개선작업이 동반되어야 하며, 이 를 위해서는 DUR시스템과 그 내용에 직접적으로 관련된 자료 분석이 필수적이 다. 따라서 본 연구의 목적은 병원정보시스템의 대규모 DDIs Date를 이용하여 약 물상호작용의 위험 요소를 인지하고, 이에 대한 의료진의 반응을 분석하여, 결 과적으로 시스템의 수용성 및 편의성을 높이기 위한 기초 정보를 제공하고자 비롯하였다. 이를 위한 단계적 목적은 다음과 같다. 첫째, DUR시스템 내에서의 DDIs 의 중복예외처방사례를 파악한다. 둘째, 내원 구분, 상병, ATC 코드에 따라 중복예외처방사례를 분석한다. 셋째, 중복예외처방사유(free text)를 그룹화하고 내원 구분, 상병, ATC 코드 별 현황을 분석, 매핑 한다.넷째, 그룹화한 사례를 근거로 수용성 및 편의성이 접목된 새로운 중복예외처 방사유 코드를 제시 한다.
C. 이론적 배경 및 선행연구
1. 의약품사용평가시스템 A) 의약품사용평가시스템의 발달 역사적으로 의약품사용평가시스템의 시작은 1960년대 초 미국의 민간보험단 체와 노인의료보험을 시행하는 주정부에서 관심을 가진 시기로 거슬러 올라간 다. 1960년대 후반, 미국 정부는 약물처방의 낮은 수준이 진료의 질을 낮출 뿐 만 아니라 약제비 지출을 불필요하게 증가시킨다는 것을 밝혀낸다. 1965년 미 국 보건후생성본부에서 의료보호관리시스템을 갖추도록 지원하게 되면서 대규 모 DUR시스템 구축을 설계하기 시작한다. 그리하여 1969년에는 DUR의 주요 목 적중 하나인 합리적인 약물처방을 통하여 보건의료의 질을 향상시키고, 불필요 한 약제비를 감소시키는 결과를 도출하게 된다(Jeong, 2006).1986년에는 병원인증 위원회에서 DUR을 의무화하였고(Choi et al., 2010), 1990년 마침내 미국의회에서는 "OBRA' 90법안 (Omnibus Budget Reconciliation Act of 1990)을 통과시키고 1993년 1월 1일까지 미국전역에 메디케이드 DUR프 로그램을 의무화하였다. 이때 구축된 DUR의 내용에는 과학적인 기준과 표준에 근거하여 의약품 사용을 할 수 있게 하고, 의약품 처방의 적절성을 평가하는 과정이 포함되도록 하였다(Chae et al., 2013).
B) 국내 의약품사용평가시스템의 발달 우리나라는 미국의 경우와는 달리 단일건강보험체계를 가지고 있어서 동시 적인 약물평가에 전산망을 활용함으로써 보다 효율적인 약물위해관리를 할 수 있었다. 이러한 가능성에 주목하여 건강보험심사평가원에서는 두 차례의 시범 사업을 토대로, 2010년 12월부터 "의약품사용평가시스템(DUR)"를 구축하고 전 국 요양기관으로 확대하였다. 우리나라 DUR 시스템은 크게 처방전내 점검과 처 방전외 점검의 두 가지로 나뉠 수 있으며, 여기서 제공되는 내용은 병용금기, 연령금기, 임부금기 의약품, 저함량 배수처방 조제의약품, 안전성관련 급여중 지의약품, 동일투여경로의 동일성분 중복처방 등이 포함 된다. 처방과정에서 병용금기, 연령금기, 임부금기(1등급, M등급 일부), 동일성분 중복처방 의약품 등으로 인하여 팝업경고창이 발생한 경우에는 그 사유를 기재한 후 처방 또는 조제를 할 수 있다. 그림 3은 DUR의 흐름도를 나타낸 것이다.
Figure 3. Workflow for Drug Utilization Review (DUR) (식품의약품안전처, 2011)
C) 전향적 DUR시스템과 후향적 DUR시스템
의약품사용평가시스템(DUR)은 의약품이 환자에게 조제되는 시점을 기준으 로, 전향적과 후향적 DUR의 두 가지로 분류될 수 있다(Choi et al., 2010). 전향적 DUR시스템은 처방전 입력단계에서 자동적으로 진행되는 것으로 약물-약 물 상호작용(drug-drug interactions, DDIs), 효능군 중복(therapeutic duplic ation, TD), 부적절한 용량과 치료기간 등을 포함한 잠재적인 문제를 사전에 파악하도록 한 것이다. 한편, 후향적 DUR시스템은 의약품이 조제되어 환자에 게 소비된 후에 수행되는 것으로서, 약물관련 이환율(Preventable Drug-Relate d Morbidity)과 같은 정보를 통해 공급자에게 약물과 관련된 정보들을 피드백 한다. 이러한 후향적 DUR 과정을 통해서 고비용 의약품 사용, 진정제나 최면제 와 같은 효능군별 의약품 사용 등에 대해 분석하게 된다(Fulda et al., 2003). 2. 선행연구 A) 약물병용금기 관련 연구 병용금기는 약물상호작용(drug interaction)으로 두 약들의 작용이 겹쳐지 면서 부작용이 생기는 것을 방지하기 위한 것이다. 잠재적인 약물-약물 상호작 용은(potential DDIs)은 가장 빈번하게 발생하는 의료사고 중 하나로서, 약물 들의 역학적인 변화가 전체적인 치료반응(overall therapeutic response)을 변 화시키는 것이다(Cho, 2003). 따라서 DDIs의 확인과정을 통해서도 약물부작용 의 상당수를 방지할 수 있다(Hansten et al., 2007). 반면 DUR 시스템은 사용자 들의 관심과 협조가 없이는 그 효과를 제대로 발휘하는데 제한이 될 수밖에 없 으며, 이러한 상황에서 약물-약물 상호작용(drug-drug interaction, DDIs)에 대한 정확한 현황 파악이 필요한 시점이다.
환자들은 치료과정에서 종종 두 가지 이상의 약물을 처방받을 수 있는데 이때 약물상호작용이 일어날 수 있으며, 이 작용은 투약된 두 약물이 상호작용을 하 여 한 약물이나 두 약물 모두의 흡수속도, 단백질결합, 생변환(bio-transforma tion), 또는 배설속도 등을 변화하도록 하는 것이다(Youn, 2005). 이러한 변화 는 부가적(additive), 시너지(synergistic), 길항적(antagonism) 등 다양한 형 태로 나타날 수 있으며, 때로는 인체에 심각한 부작용과 독성을 일으킬 수도 있다. 따라서 DDIs은 빈번하게 발생하는 의료사고중 하나이며(Enna et al., 199 7), DDIs의 확인과정을 통해서도 약물부작용의 상당수를 방지할 수 있게 된다 (Hansten et al., 2007). 우리나라 DUR에서는 병용금기 의약품의 지정을 복지부 에서 고시하고 식약청에서 공고한 성분들로, 동시 투약하면 안 되는 의약품에 대해서 처방전내와 처방전간의 두 가지 시스템으로 점검한다. 만약 병용금기 약 임에도 처방하는 경우에는 그 예외사유를 제공되는 코드들 중에서 선택하여 입력하게 되는데, 적절한 코드항목이 없을 경우에는 자유롭게 서술, 기재하여 그 내용을 전송해야 한다(Choi et al., 2010). B) 중복처방에 따른 약물상호작용 위험 관련 연구 약물의 상호작용에는 한 약물과 다른 종류의 약물이 동시에 투여될 때 효과 가 발생하는 경우를 의미한다. 약물상호작용에는 병용약물에 의해서 처방된 약 물이 상호 작용을 하거나 상승작용을 함으로써 치료효과가 원래 의도했던 것보 다 올라가면서 독성의 저하, 부작용의 감소 등이 발생하는 유익한 상호작용도 있다(McCarthy, 2003). 반면 길항작용에 의해 치료 작용이 감소되면서 질병의 상태가 악화 되거나 상승작용으로 인한 약물작용이 지나치게 상승하게 됨으로 써 부작용 또는 중독 작용이 발생하는 유해한 상호작용도 있다(신순식 외, 2000). 기본적으로 투약되는 약제의 종류가 적을수록 예상하지 못한 부작용이나 약물 상호작용에서 안전하다. 하지만 만성 질병의 증가와 합병증의 증가, 노인인구
의 증가 등으로 인하여 현재에는 많은 종류의 신약이 개발되고, Herbal제도가 증가하면서 다 약제처방과 복용이 빈번해지고 있다. 따라서 약물 간 상호작용 의 범위도 확대되고 있는 실정이다(홍경자,이석용, 2003). 약물상호작용으로 인한 약물부작용의 증가는 65세 이상의 위험집단인 고령인구와, 신체발달이 아 직 완전히 이루어지지 않은 유, 소아에서 특히 더욱 심각할 수 있으며, 이로 인한 이차적인 치료로 인하여 경제적인 손실 문제도 증가 하고 있다(이승환 외, 2015). 우리나라에서는 2004년에 보건복지부 고시로 1차 162품목을 2005년에는 2차 42품목으로 총 204품목이 약물조합의 병용금기 성분으로 지정된 바 있다(보건 복지부, 2004; 보건복지부, 2005). 이때 고시된 성분들의 조합은 미국의 DUR에 서 사용되던 National Drug Data File 중에서 DDIM(Drug-Drug Interaction Module)을 근거로 하였다. 이에 약물상호작용 1등급으로 분류되어 있던 약물의 조합에서 대부분 도입하였으며, 성분조합 중에서 일부는 우리나라 식약청 허가 정보를 기준으로 하였다. 그리고 함께 복용 하였을 시 국민건강상 위해가 있다 고 지정을 하였음에도 동시 투약을 할 경우에는 보험급여를 인정하지 않게 하 였다(유경진외, 2005). 또한 병용금기 고시성분은 병용할 때 발생하는 타약제 의 효능, 대사, 배설 등의 전반적인 과정에 미치는 영향을 고려하여 결정된다. 중복약물의 조합은 내용에 따라 그 위해도가 다를 수 있다. 이는‘Drug Intera ction Facts(2006)’의 평가지침서에서 약물과 약물, 약물과 음식, 약물과 알 코올 등의 상호작용에 대한 정보와 그 중요도에 대해서 설명해 준다(조진환, 2 005). 여기에서는 Significance Rating을 1~5등급까지 있으며 그 위중의 정도 에 대한 정보를 담고 있다. 예를 들어 Significance 1 은 생명을 위협할 수 있 을 정도로 상호작용의 정도가 위험한 것으로서 약물동력학적으로 영구적인 손 상을 가져올 수 있다고 상호작용이 확인된 것이고, Significance 2 는 환자의 질병상태를 악화시키는 중증도의 위험단계인데, 이 경우 추가적인 치료나 입원 또는 재원기간의 연장이 필요해진다. Significance 3 은 상호작용이 가장 약한 등급인데 약물동역학적으로 확인되었거나 또는 약리작용변화가 일어날 가능성
이 있으며, 이는 아직 불명확하고 치료결과에 대해 유의한 영향을 미치지 않는 경우이다(표 3).
Significance
Rating Severity Documentation 1 Major Suspected or further 2 Moderate Suspected or further 3 Minor Suspected or further 4 Major/Moderate Possible
5 Minor Possible Any Unlikely
Table 3. The significance ratings of drug interactions
병원 현장에서 Significance에 따른 경고문의 의미는 선행연구를 통하여 보고 된 바 있다. 이 정화(2006)는 3차 병원의 외래환자 처방의 약물상호작용을 Sig nificance Rating 평가하였으며, Significance Rating을 1~3등급에 해당하는 약물 조합 중에서 연구대상이었던 고려대의료원에서 처방이 가능한 약품들로 조합하여 1,069개의 조합을 만들었으며, 동일 처방전과 투약일수가 중복된 다 른 처방들과의 EMR 을 분석 검토 하였다. 분석 결과 1년 동안 2종이상의 약물 로 중복 처방된 처방전은 287,905(58.8%)였는데, 이중 107,663건(37.4%)는 60~ 80세 사이의 고령층에서 가장 많이 처방되고 있었다. 이어서 40~60대가 100,72 0건(35%)이였고 이러한 비율은 본 연구에서의 중복처방에 따른 연령분석과 유 사한 결과였다. 참고로 이 정화(2006)의 연구에서는 Significance 1 은 245개 약물들 사이에서, Significance 2 는 732개 약물들 사이에서, Significance 3 은 92개 약물들 사이에서 조합을 만들었다. 그리고 이들 위험도에서 상호작용 약물조합은 1년간 총 57,689건이 처방되었는데, 이 중 Significance 1에서는 4,640건(25.4%), Significance 2 에서는 31,932건(55.4%), Significance 3 은 11,117건(19.3%)인 것으로 나타났다.
Drug-related factors Patient-related factors Ÿ Narrow therapeutic range
Ÿ Low bioavailability Ÿ Drug formulation Ÿ Stereochemical and
physiochemical properties Ÿ Drug potency
Ÿ Steep dose-response curve Ÿ Treatment duration (acute or
chronic administration) Ÿ Dosage (a higher dosage
increases the chance of drug interaction)
Ÿ Treatment timing and method (concurrent or staggered administration)
Ÿ Administration route
Ÿ Baseline blood levels of drugs and therapeutic ranges
Ÿ Extent of drug disposition and rate of drug metabolism
Ÿ Protein binding
Ÿ Volume of distribution
Ÿ Body weight and body mass index
Ÿ Amount and activity of specific drug-metabolizing enzymes in organs (due to genetic
polymorphism)
Ÿ Inter individual variability in pharmacokinetics and pharmacological responses to drug Ÿ Gender Ÿ Age Ÿ Ethnicity Ÿ Diet
Ÿ Underlying disease states and their severity
Ÿ Dysfunction or disease of drug Ÿ metabolizing organs (e.g.,
kidney, liver) Ÿ Poly pharmacy
Table 4. Factors related to drug–drug interaction
CYP3A, cytochrome P450 subfamily 3A; MTX, methotrexate; NSAIDs, non-steroidal anti-inflammatory agents (Scripture and Figg, 2006)
Class of medication that interacts with
chemotherapy
Examples of interactions
Antacids Antacids that contain aluminum and magnesium can increase the bioavailability of capecitabine Antibiotics
Penicillins block the elimination of MTX through renal tubular secretion, which results in elevated MTX levels
Anticoagulants
Altered coagulation has been reported in patients who have taken warfarin concurrently with
capecitabine
Anticonvulsants Carbamazepine may increase systemic clearance of teniposide
Antiemetics
Co-administration of ondansetron with cisplatin and cyclophosphamide can lead to a decrease in systemic exposure to both cisplatin and
cyclophosphamide Antifungal agents
Ketoconazole inhibits the metabolism of irinotecan, which can lead to an increase in exposure to SN-38 (the active metabolite of irinotecan)
Antiretroviral agents
Co-administration of delavirdine and saquinavir with paclitaxel can result in severe paclitaxel toxicity, which is possibly caused by inhibition of CYP3A activity
Corticosteroids Corticosteroids decrease the anti-tumor efficacy of aldesleukin Corticosteroids Corticosteroids decrease the anti-tumor efficacy
of aldesleukin Herbal supplements
St John’s wort decrease the plasma concentration of imatinib
and SN-38 (the active metabolite of irinotecan) NSAIDs
NSAIDs block the elimination of MTX through renal tubular secretion, which results in elevated MTX levels
Ⅱ. 연구방법
A. 연구대상 자료 분석
우리나라 의약품사용평가시스템(Drug Utilization Review, DUR)에 내장된 DDIs의 예외사유코드 A~C, F~K, P로 모두 11종류이며, 여기에 더해서 병용, 연 령, 임부와 관련하여 text로 중복처방 사유를 자유롭게 입력할 수 있도록 하고 있다. 본 연구에서는 2012년 4월부터 2013년 1월15일까지 아주대학교 의료원을 내원한 외래 환자처방 건수 중 DDIs의 중복 예외사유코드로 입력된 총 7,772건 과, 외래, 입원, 응급 등 총 환자들 중 예외처방사유(자유진술문)에 입력된 총 89,686건을 대상으로 분석하였다(표 6). 자유진술문 중 외래환자 건수는 총 20,183건, 입원환자는 41,861건, 응급 등 기타는 27,642건이었다. 중복예외처방코드의 분석에 사용된 7,772건은 모두 외 래환자로만 구성되어 있다(표 6 ,그림 5). 또한, 외래 환자들 중 중복예외처방코드 7,772건과 외래, 입원, 응급 및 기타 의 중복예외처방사유로 입력한 89,686건을 입력된 내용을 빈도에 근거하여 13 개 그룹으로 분류를 한 후 ATC코드와 ICD코드, 연령 등을 포함하여 빈도분석과 교차분석을 실시하였다.
중복예외처방사유내용 분류는 Grizzle et al.(2007)와 Ahn et al.(2014)의 예 외처리 코드를 참고하여 작성하였다. 이는 Grizzle et al.(2007)의 연구에서 DDI경고를 없애기 위해 14가지 분류를 만들었고, 분류(규정)자 들은 이동성 약 물학적 투여 조제 레코딩으로부터의 복제를 배제시킨 후 카테고리를 만들어 사 용된 코드를 기초로 하여 적용하였고, 또한 텍스트 분류 pilot test 중 필요한 코드는 Ahn et al.(2014)의 연구가 우리나라 상황에서 도출된 코드이기에 이를 참고로 연구를 수행 하였다.
Chicago, IL, USA)를 이용하였다. 또한, 처방의사가 건강보험심사평가원 (Health Insurance Review & Assessment Service, HIRA)이 제공하는 중복예외 처방 코드를 사용한 경우와 코드에 입력하지 않고 자유진술문으로 입력한 모든 건을 3명의 독립적인 연구자가 직접 수작업(manual work)으로 평가하여 새로 분류하고 기존(HIRA)의 코드와 비교하였다.
Overlapping
prescription code Reasons for override Total (N,%) Outpatient 7,772 (100.0) 20,183 (22,5) 27,955(28,6)
Inpatient - 41,861 (46.7) 41,861(43,0)
Emergency and
other causes - 27,642 (30.8) 27,642(28,4)
Total 7,772 (100.0) 89,686 (100.0) 97,458 (100.0) Table 6. Subject groups
그림 4 는 외래, 입원, 응급 및 기타의 모든 중복 예외 처방사유 98,829 건에 대해 Date Cleansing 한 최종 97,458 건을 코드 7,772 건(외래)과 자유진술문 (Free-text) 89,686건으로 분류한 다음 사유 내용을 13개 그룹으로 그룹화 하 여 분석한 후 기존 HIRA 코드11개와 매핑 하여 새로운 코드 6 개를 도출 하였 다.
Figure 4. Study framework
그림 5 는 전체 데이터에 대한 분석의 경우 최초 중복예외처방코드(reasons for override(coded))로 입력된 건수 7,879건 중 결측치 48건, 알 수 없는 의 약품 정보로 입력된 건수 59건을 제외한 7,772건이 최종 선택되었고, 최초 외 래, 입원, 응급 환자 및 기타(reasons for override(free text))로 입력된 90,950 건 중 결측치 360건, 알 수 없는 의약품 정보로 입력된 904건을 제외한 89,686건이 최종 선택되었다. 분석 결과, 응급 및 기타환자에 대한 결측치와 알 수 없는 의약품 정보로 입력된 건수가 현저히 낮음에 원인분석 및 추가연구 의 필요함이 제기 된다. 이에 대한 결측치란 환자의 정보(연령 또는 성별, 진 단코드 등) 및 의약품 정보가 없는 자료이며, 의약품 분류가 명확하게 되지 않
은 경우는 약품이 일반적으로 사용되는 성분 명 또는 제품명이 아닌 텍스트로 쓰여 진 경우 또는 의약품 DB(건강보험심사평가원 의약품 데이터베이스 및 KIMS 의약정보센터(https://www.kimsonline.co.kr/)에서 검색이 불가한 자료로 데이터에서 제외하였다. 이에 따라 최초 98,829건 중 본 연구의 분석을 위해 사용된 최종 자료는 97,458건이다.
B. 연구대상 비교 코드
본 연구에서 분석하고자 하는 ATC code는 의약품 분류코드 (Anatomical Therapeutic Chemical Code)로서 세계보건기구(WHO) 산하 기관인 Drug Statistics Methodology(WHOCC)에서 정하며 약물의 신체 내 기관에 따른 약물 의 활성에 근거하여 5단계에 의해 분류하고 있으며, 각 단계별 분류 집단은 다 음과 같다. 1 단계는 해부학적 주요 그룹을 1 개의 영문자로 지정 하였고 14개의 주요 그 룹은(표 7)와 같다. 2 단계는 2 개의 숫자로 구성되며 주요 치료적 그룹을 지정한다. 3 단계는 1개의 영문자로 구성된 치료적/약물학적 하위그룹을 지정한다. 4 단계는 1개의 영문자로 화학적/치료적/약물학적 하위그룹을 지정한다. 5 단계는 2개의 숫자로 구성된 화학물질을 지정한다. 본 연구에서는 ATC코드 의 첫 번째 단계 (세 자리), 즉, 해부학적 정보를 가진 치료적 그룹을 기준으 로 처방 약물을 분류 하여 비교 분석 하였다.
Code Contents A Alimentary tract and metabolism B Blood and blood forming organs C Cardiovascular system
D Dermatologicals
G Genito-urinary system and sex hormones
H Systemic hormonal preparations, excluding sex hormones and insulins
J Anti-infectives for systemic use
L Anti-neoplastic and immunomodulating agents M Musculo-skeletal system
N Nervous system
P Anti-parasitic products, insecticides and repellents R Respiratory system
S Sensory organs V Various
Table 7. Fourteen Anatomical Main Groups of the First Level of the ATC Codes
The first level of each code indicates the anatomical main group and comprises one letter. There are 14 main groups.
ATC, Anatomical Therapeutic Chemical classification
본 연구에서 분석하고자 하는 국제질병분류코드인 ICD(international classif ication of disease) 코드는 세계보건기구에 의해 정해진 국제적으로 통용되는 역학적인 건강조절과 임상적인 목적에 대한 표준 진단 도구이다.
III. 연구결과
A. 외래환자의 중복 예외처방코드(HIRA) 분석결과
1. 월별 분석
연구대상 병원의 외래 환자들 중 의약품 사용평가시스템(Drug Utilization Review, DUR)의 DDIs 중복 예외처방을 분석하기 위하여 추출한 중복예외처방코 드는 7,772건이었다. 외래 환자들 중 예외처방코드의 경우 7,772건을 분석 하 였을 때, 월별로 DUR에 약물-약물상호작용(Drug-Drug Interactions, DDIs)로 기록된 수는 급격히 차이가 났다. 2012년 4월부터 9월까지 500명 미만으로 큰 변동이 없다가 10월, 11월에 1천여 건이 기록된 후 12월에 2,998건으로 급격히 증가하고, 그런 다음 2013년 1월에는 다시 1,507건으로 12월에 비해 25%정도가 감소하고 있었다. 따라서 이러한 추세가 매년 일정한 경향성을 띠는지를 확인 하기 위해서는 보다 장기적인, 그리고 다른 연도의 자료와의 비교가 필요하다.
2. 연령별 분석
DDIs에 기록된 외래환자의 연령대는 0세에서 90대까지였으며, 50대가 가장 많은 22.1%였고, 그 다음으로 60대가 20.2%, 그리고 40대가 15.6%여서, 40대부 터 60대까지가 전체의 57.9%를 차지하고 있었다(그림 6, 표 8).
Figure 6. Age Distribution
Age Frequency Percentage -9 165 2.1 10-19 131 1.7 20-29 397 5.1 30-39 693 8.9 40-49 1,215 15.6 50-59 1,716 22.1 60-69 1,567 20.2 70-79 1,475 19.0 80-89 380 4.9 90- 32 0.4 Total 7,772 100.0
3. DDI의 중복예외처방 코드(HIRA) 빈도분석 DDIs의 외래환자의 중복예외처방 코드의 빈도를 분석 하였을 때 가장 높은 비율을 차지하고 있었던 것은 A와 F로서 각각 31.2%와 32.4%를 차지하고 있어 서 이 두 항목 만으로 63.6%를 차지하고 있었다. 이외에 10%이상을 점유하는 항목은 I 하나였다(표 9, 그림 7). Code Contents N % A
When a patient has to receive a prescription before exhausting the existing medicine or medical supplies due to a long-term business trip or travel
2,428 31.2 B
When specific ingredients cannot be sorted for separate prescriptions among existing prescribed medicine due to preparation in powder form
64 .8 C
When medicine is destroyed or altered for reasons not attributable to the patient (e.g., vomiting during drug intake)
377 4.9 F When the prescription and administration dates differ 2,518 32.4 G When a medicine is administered weekly or monthly 490 6.3 H When overlapping or combined drug use occurs by changing only the method of intake or volume 621 8.0 I When overlapping or combined drug use occurs by changing the number of administration dates 785 10.1 J When a patient does not take the existing prescription or prepared drug (voluntarily) 79 1.0 K When a patient cannot reach the prescribing doctor or preparing pharmacists via phone 1 .0 L When a patient is not permitted to take the existing prescribed medicine (by the doctor) 197 2.5 P When a medicine is administered pro re nata (PRN) 211 2.7 Total 7,772 100.0
Table 9. Frequency of Overlapping Prescription Codes Among the 7,772 Outpatient Cases (Grounds for the Report)
4. ATC코드 빈도분석
ATC코드는 총 14개 항목으로 분류를 하는데, 빈도분석을 하였을 때, A가 21.5%, C가 21.1%, 그리고 N이 27.4%였는데 이들 세 항목을 합하면 모두 70%를 점유하고 있었다(표 10).
*The results of the second level (three digits) of the ATC are included in supplementary 1.
ATC, Anatomical Therapeutic Chemical classification
Code Category N % Major drugs A Alimentary tract
and metabolism 1,668 21.5
Stomach acid, antacids, H2 antagonists, proton pumps, antiemetics, laxatives, antidiarrheal drugs, vitamins B Blood and blood-forming organs 680 8.8
Antithrombotic agents, antiplatelet agents, anticoagulating agents, clot busters, antianemic agents, platelets, coagulating agents
C Cardiovascular
system 1,643 21.1
Antianginal agents, diuretics, vasodilators, beta blockers, calcium channel blockers, renin angiotensin system, ACE inhibitors, angiotensin II
D Dermatologicals 124 1.6 Malactic agents, cicatrizing agents, antipruritic agents, antipsoriatic agents
G
Genito-urinary system and sex
hormones
142 1.8
Hormone contaceptives, fertility agents, selective estrogen receptors, regulatory hormones H Systemic hormonal preparations, excluding sex hormones and insulins 322 4.1
Hypothalamic-hypophyseal hormones, steroid hormones, thyroid hormones, antithyroid hormones
J Antiinfectives for
systemic use 72 0.9
Antimicrobial agents, antiviral agents, antiparasitic agents, intravenous immunoglobulin vaccines
L
Antineoplastic and immunomodulating
agents
186 2.4 Anticancer agents, metabolic antagonists, immunomodulators, immunostimulators
M Musculoskeletal
system 303 3.9
Anabolic steroids, antiinfectives, NSAIDs, antirheumatic agents, corticosteroid muscle relaxants
N Nervous system 2,130 27.4 Analgesic agents, anesthetics, anticonvulsant agents, antidepressants, antianxiety agents P Antiparasitic products, insecticides and repellents 111 1.4
Antimicrobial agents, antiviral agents, antiparasitic agents, intravenous immunoglobulin vaccines
R Respiratory system 360 4.6 Anti-inflammatory agents, bronchodilator, antitussive agents
S Sensory organs 8 0.1 Ophthalmology, otology
V Various 22 0.3 Detoxicants, contrast agents, dressings for radiological pharmacology
Total 7,772 100
Table 10. Frequency of ATC Codes among the 7,772 Outpatient Cases with Overlapping Prescription Codes (Grounds for the Report)
5. ICD 코드 빈도분석
질병의 국제분류(International Classification of Diseases: ICD)는 질병 을 모니터링하고 기록하는데 있어서 세계적인 공통언어로서 중요한 의미를 갖 는다. 이러한 표준적인 방법을 통하여 지역과 국가 그리고 병원들 간의 정보를 시간을 달리하면서도 공유하고 비교할 수 있다. 그리고 데이터를 분석하고 선 별하고 정책을 입안할 때에도 이 증거에 기반 한 의사결정을 하도록 돕는다(유 경진 외, 2005). 7,772건의 외래환자들 중 중복사유가 메뉴에서 선택된 예외사유코드를 분석 하였을 때, ICD코드를 기준으로 DDIs의 빈도가 F: 12.2%, I: 19.5%, M: 16.5% 로 이 세 항목으로 모두 48.2%를 차지하였다. 이어서 G: 9.3%, E: 8.9%였다. 즉, 총 20항목 중 F, I, M, G, E의 다섯 항목이 총 75.3%로서 전체의 3/4을 차 지하였다(표 11).
ICD code Contents N %
Missing value 1 .0
A Certain infectious and parasitic diseases 34 .4 B Certain infectious and parasitic diseases 89 1.1
C Neoplasms 426 5.5
D Diseases of the blood and blood-forming organs and certain disorders involving the
immune mechanism 122 1.6
E Endocrine, nutritional, and metabolic
diseases 693 8.9
F Mental and behavioral disorders 950 12.2
G Diseases of the nervous system 721 9.3
H Diseases of the eye and adnexa/Diseases of the ear and mastoid process 103 1.3 I Diseases of the circulatory system 1,519 19.5 J Diseases of the respiratory system 219 2.8 K Diseases of the digestive system 242 3.1 L Diseases of the skin and subcutaneous
tissue 160 2.1
M Diseases of the musculoskeletal system
and connective tissue 1,283 16.5
N Diseases of the genitourinary system 436 5.6 P Certain conditions originating in the
perinatal period 6 0.1
Q Congenital malformations, deformations, and chromosomal abnormalities 49 0.6
R
Symptoms, signs, andabnormal clinical and laboratory findings, not elsewhere
classified
434 5.6
S Injury, poisoning, and certain other
consequences of external causes 54 0.7 T Injury, poisoning, and certain other
consequences of external causes 32 0.4 Z Factors influencing health status and
relationships with health services 198 2.5
Total 7,772 100.0
Table 11. Frequency of ICD codes among the 7,772 Outpatient Cases with Overlapping Prescription Codes
*Detailed results are included in supplementary 2
ICD, International Statistical Classification of Diseases and Related Health Problems
6. ATC 코드와 중복예외처방(HIRA)코드의 교차분석
중복 예외처방 코드에 따른 약물의 종류를 확인하기 위하여 교차분석을 시 행하였다. 앞서 분석한 ATC코드 중 가장 빈도가 높았던 A,C,N 항목을 확인 하 였을 때, ATC코드 A는 중복예외처방 코드 A와 F가 각각 37.1%와 31.7%를 차지 하였으며, ATC코드 C도 각각 35.2%와 36.6%, 그리고 ATC코드 N은 23.7%와 30.3%를 차지하고 있었다. 즉, 질병의 종류에 무관하게, 중복처방 되는 경우는 A: 환자가 장기출장이나 여행 등으로 인하여 미리 처방받는 경우와 , F: 처방 일과 투약일이 달라서 실제로는 중복복용을 하지 않는 경우였다. 중복예외처방 코드 중 실제로 환자에게 중복 투여되는 경우는 B: 분말 등의 형태로 제조되기 에 특정성분만을 분리할 수 없는 경우와 P: 필요시 투약하는 약제이다. 따라 서 DDIs로 인한 사후관리와 보고가 필요한 경우는 B의 64회와 P의 211회가 된 다. 이어서 ATC코드와 중복예외처방코드 B와 P를 교차분석으로 확인 하였을 때, 가장 많은 빈도를 차지한 것은 ATC코드 N (뇌와 신경계)과 R(호흡계)에서 중복예외처방 코드 P(상황에 따라)의 각각 67회와 60회였으며, 이어서 ATC코드 A(대사)와 C(심혈관계)의 각각 32회, 25회였다. 한편 중복예외처방 코드 B에서 는 ATC코드 C (심혈관계)에서 29회가 가장 높았다(표 12).
ATC, Anatomical Therapeutic Chemical classification 7. ICD코드와 중복예외처방코드(HIRA)의 교차분석 P와 B를 중심으로 ICD코드의 교차분석을 확인해보면 가장 높은 빈도는 ICD 코드 J(호흡계)과 M번(근골격계)의 P(필요에 따라)가 각각 46회와 34회로 가장 많았으며, 이어서 ICD I(순환계)과 R(기타)의 B(분말 등으로 혼합)가 각각 25 회와 16회를 차지하고 있었다(표 13).
ATC code Overlapping Prescription Codes
B P A 10 32 B 9 7 C 29 25 D 0 2 G 0 5 H 9 3 J 0 0 L 0 5 M 1 5 N 4 67 P 0 0 R 2 60 S 0 0 V 0 0 Total 64 211
Table 12. Cross Tabulation of ATC Codes and Overlapping Prescription Codes B and P
ICD, International Statistical Classification of Diseases and Related Health Problems
ICD code Overlapping Prescription Codes
B P A 0 4 B 11 9 C 0 3 D 2 1 E 1 11 F 1 13 G 0 2 H 2 0 I 25 14 J 2 46 K 0 5 L 0 19 M 1 34 N 0 16 P 0 0 Q 0 0 R 16 0 S 0 16 T 0 11 Z 3 7 Total 64 211
Table 13. Cross Tabulation of ICD Codes and Overlapping Prescription Codes B and P
B.외래, 입원, 응급, 기타의 중복예외처방사유(Free-text)분석
결과
1. 전체 중복예외처방사유내용(13개 분류) 분석 연구기간 동안 외래, 입원, 응급 등에서 총 89,686건이 시스템 내에 선택항 목이 존재하지 않아서 자유로운 문장으로 DDIs의 이유를 서술하였다. 이에 대 한 분류를 하였을 때, 가장 높은 비율을 차지한 것은 같은 시간대 투약이 아닌 경우가 31.6% (28,306회)로 나타났으며, 이어서 질병이나 증상을 표기한 것 (19,909회)이 22.2%를 차지하고 있었다. 염증항목은 열, 부종, 통증, 감염 등 의 항목을 포함한 것으로서 총 13.1% (17,020회)를 차지하고 있었다. 전혀 의 미가 없는 ‘ㅋㅋㅋ’와 같은 형식으로 표기된 것도 12% (10,741회)나 되었으 며, 단어나 문장을 서술하였으나 어떤 의미인지 확인하기가 어려운 불분명한 표기도 0.6%(575회)를 차지하고 있는 것으로 분석되었다(표 14). Causes of override N % Pro re nata 1,799 2.0 Name of the disease or symptoms 19,909 22.2 Doctor’s name or instructions 3,222 3.6 Drug name 1,770 2.0 Emergency 346 .4 System error 8 .0 Inflammation 11,720 13.1 No specific meaning 10,741 12.0 Not to be taken orally 964 1.1 Not to be taken at the same time 28,306 31.6 Related to surgical operations 1,873 2.1 Benefits exceed dangers 8,418 9.4 Ambiguous reasoning 575 .6 Total 89,686 100.02. 연령과 중복예외처방사유(Free-text)분석 중복예외처방사유(Free-text)을 표 15와 같이 13개 항목으로 나눈 후 연령 별로 교차분석을 진행하였을 때 가장 많은 빈도를 차지한 것은 40대와 50대로 모두 각각 17%를 차지하고 있었다. 이어서 30대 (14.5%)와 60대 (13.3%)가 많 았다. 각 연령별로 주요 예외사유내용의 항목들의 내용이 달랐다. '필요에 따 라'항목에서 높은 비율을 차지한 연령대는 60대 (22.9%), 50대(19.0%), 70대 (17.2%)의 순 이였으며, 염증비율이 높은 연령대는 40대(15.4%), 30대(13.8%), 60대(13.2%)의 순이었다. 주목할 만한 예외사유내용항목은 '아무 의미 없음' 항목이었다. '아무 의미 없음' 항목은 'ㅋㅋㅋ', '11111' 와 같이 어떤 의미 없이 예외사유 내용 란을 단순한 철자나 단어 숫자 등을 채워 넣은 것을 말한 다. 본 연구에서 총 89,686건이 기록된 예외사유내용 중에서 '아무 의미 없음' 은 10,740건인 12.0%를 나타냈다. 대부분의 예외사유내용 항목들이 가장 높은 비율을 차지한 것이 30대에서 70 대 사이였던 반면에 '아무 의미 없음'항목이 가장 높은 빈도를 나타낸 연령대 는 10세 미만의 연령대로서 전체 '아무 의미 없음' 중 20.2%를 차지하고 있었 다. 이어서 50대(15.3%), 60대(14.9%), 70대(14.0%)의 순으로 나타났다. 모든 연령대에서 약물중복의 위험성은 있지만, 특히 간이나 신장을 포함한 인체 기 관들이 완전히 발달되지 않은 영유아가 포함된 10대 미만의 연령대에 약물부작 용으로 인한 영향을 매우 크고 치명적일 수 있다. 그러함에도 '아무 의미 없음 '의 가장 높은 비율이 10대 미만이라는 사실은, 약물처방의 과정에서 10대 미 만의 경우 더욱 주의를 기울일 필요를 함축한다. '위급한 상황'항목에서 가장 높은 비율을 차지한 것은 60대(37.9%)와 70대 (28.3%)로서 이 두 연령대의 합만으로 66.2%를 차지하고 있었다. 따라서 위급 한 상황과 관련된 약물의 중복처방의 과정과 사후관리에서 60대와 70대를 중점 적으로 관심을 둘 필요가 있다.
Age groups
1-9 10-19 20-29 30-39 40-49 50-59 60-69 70-79 80-89
90-Pro re nata N 108 47 56 187 210 319 384 289 74 5
% 1.3 .9 .6 1.4 1.4 2.1 3.2 3.1 3.0 2.0
Name of the disease or symptoms N 1,726 263 789 2,354 4,500 5,081 3,087 1,710 373 24 % 21.0 5.2 8.9 18.1 29.5 33.3 25.9 18.1 15.2 9.4 Doctor’s name or instructions N 140 87 168 309 417 642 545 658 235 21 % 1.7 1.7 1.9 2.4 2.7 4.2 4.6 7.0 9.5 8.2 Drug name N 107 46 21 304 187 249 233 423 174 26 % 1.3 .9 .2 2.3 1.2 1.6 2.0 4.5 7.1 10.2 Emergency N 42 13 1 3 9 22 131 98 20 7 % .5 .3 .0 .0 .1 .1 1.1 1.0 .8 2.7 System error N 0 0 0 0 4 2 0 1 1 0 % .0 .0 .0 .0 .0 .0 .0 .0 .0 .0 Inflammation N 1,685 883 900 1,620 1,809 1,473 1,548 1,407 367 28 % 20.5 17.5 10.2 12.4 11.9 9.6 13.0 14.9 14.9 11.0 No specific meaning N 2,165 555 542 1,023 1,339 1,643 1,596 1,501 348 28 % 26.4 11.0 6.1 7.9 8.8 10.8 13.4 15.9 14.1 11.0 Not to be taken orally N 243 25 39 41 91 164 136 143 72 10 % 3.0 .5 .4 .3 .6 1.1 1.1 1.5 2.9 3.9 Not to be taken at the same time
N 976 2,700 5,891 6,322 5,404 3,640 1,908 1,300 249 36 % 11.9 53.6 66.6 48.6 35.4 23.8 16.1 13.8 10.1 14.1 Related to surgical operations N 202 134 107 152 245 311 379 295 44 4 % 2.5 2.7 1.2 1.2 1.6 2.0 3.2 3.1 1.8 1.6 Benefits exceed dangers N 759 256 283 658 931 1,601 1,851 1,538 496 45 % 9.2 5.1 3.2 5.1 6.1 10.5 15.6 16.3 20.2 17.6 Ambiguous reasoning N 57 28 40 45 112 122 100 62 8 1 % .7 .6 .5 .3 .7 .8 .8 .7 .3 .4 Total N 8,210 5,037 8,838 13,018 15,258 15,269 11,898 9,440 2,461 255 % 100.0 100.0 100.0 100.0 100.0 100.0 100.0 100.0 100.0 100.0
3. ICD코드와 중복예외처방사유(Free-text)분석 ICD코드는 국제적으로 통용되는 기호이다. 총 예외사유내용 가운데 가장 높은 비율을 차지한 ICD코드는 M코드로서 23.6%(21,183건)를 차지하고 있었다 (표 16). M코드 다음으로는 J 가 11.5%, 그리고 K (10.1%)가 뒤를 이었다. 5% 미만을 차지한 코드는 A, B, D, E, F, G, H, L, O, P, Q였으며, U, V, W, X, Y 는 25건 미만으로 0%대를 차지하였다.
Group Total Pro re nata Name of the disease or symptoms Doctor’s name or instructions Drug name Emergency System error Inflammation No specific meaning Not to be taken orally Not to be taken at the same time Related to surgical operations Benefits exceed dangers Ambiguous reasoning ICD A N 24 387 94 24 21 0 8 410 4 500 30 129 12 1,645 ICD % 1.5 23.5 5.7 1.5 1.3 .0 .5 24.9 .2 30.4 1.8 7.8 .7 100.0 group % 1.4 1.9 2.9 1.4 6.1 .0 6.7 3.8 .4 2.2 1.6 1.5 2.1 1.8 Total % .0 .4 .1 .0 .0 .0 .0 .5 .0 .6 .0 .1 .0 1.8 B N 15 131 29 2 1 0 1 138 7 189 5 88 29 635 ICD % 2.4 20.6 4.6 .3 .2 .0 .2 21.7 1.1 29.7 .8 13.9 4.6 100.0 group % .9 .7 .9 .1 .3 .0 .8 1.3 .7 .9 .3 1.0 5.0 .7 Total % .0 .1 .0 .0 .0 .0 .0 .2 .0 .3 .0 .1 .0 .7 C N 155 1,687 189 99 32 2 20 1,259 39 2,190 69 635 103 6,480 ICD % 2.4 26.0 2.9 1.5 .5 .0 .3 19.4 .6 33.8 1.1 9.8 1.6 100.0 group % 9.2 8.5 5.9 5.6 9.2 25.0 16.7 11.7 4.0 8.7 3.7 7.5 17.9 7.2 Total % .2 1.9 .2 .1 .0 .0 .0 1.4 .0 2.4 .1 .7 .1 7.2 D N 29 349 83 16 4 0 4 292 6 1,813 55 130 3 2,785 ICD % 1.0 12.5 3.0 .6 .1 .0 .1 10.5 .2 65.1 2.0 4.7 .1 100.0 group % 1.7 1.8 2.6 .9 1.2 .0 3.3 2.7 .6 6.5 2.9 1.5 .5 3.1 Total % .0 .4 .1 .0 .0 .0 .0 .3 .0 2.0 .1 .1 .0 3.1 E N 109 297 14 17 3 0 3 177 8 428 7 212 8 1,283 ICD % 8.5 23.1 1.1 1.3 .2 .0 .2 13.8 .6 33.3 .5 16.5 .6 100.0 group % 6.5 1.5 .4 1.0 .9 .0 2.5 1.6 .8 1.7 .4 2.5 1.4 1.4 Total % .1 .3 .0 .0 .0 .0 .0 .2 .0 .5 .0 .2 .0 1.4 F N 4 98 31 0 1 0 0 49 3 154 7 76 3 426 ICD % .9 23.0 7.3 .0 .2 .0 .0 11.5 .7 36.1 1.6 17.8 .7 100.0 group % .2 .5 1.0 .0 .3 .0 .0 .5 .3 .8 .4 .9 .5 .5 Total % .0 .1 .0 .0 .0 .0 .0 .1 .0 .2 .0 .1 .0 .5 G N 110 673 249 34 28 0 2 943 13 1,472 113 346 12 3,995
Group Total Pro re nata Name of the disease or symptoms Doctor’s name or instructions Drug name Emergency System error Inflammation No specific meaning Not to be taken orally Not to be taken at the same time Related to surgical operations Benefits exceed dangers Ambiguous reasoning ICD % 2.8 16.8 6.2 .9 .7 .0 .1 23.6 .3 36.8 2.8 8.7 .3 100.0 group % 6.6 3.4 7.7 1.9 8.1 .0 1.7 8.8 1.3 7.1 6.0 4.1 2.1 4.5 Total % .1 .8 .3 .0 .0 .0 .0 1.1 .0 1.6 .1 .4 .0 4.5 H N 3 370 55 6 6 0 0 166 2 658 22 129 4 1421 ICD % .2 26.0 3.9 .4 .4 .0 .0 11.7 .1 46.3 1.5 9.1 .3 100.0 group % .2 1.9 1.7 .3 1.7 .0 .0 1.5 .2 3 1.2 1.5 .7 1.6 Total % .0 .4 .1 .0 .0 .0 .0 .2 .0 .8 .0 .1 .0 1.6 I N 222 1,767 244 41 38 0 12 1,019 43 2,281 117 572 108 6,488 ICD % 3.4 27.2 3.8 .6 .6 .0 .2 15.7 .7 35.2 1.8 8.8 1.7 100.0 group % 13.2 8.9 7.6 2.3 11. .0 10.0 9.5 4.5 8.9 6.2 6.8 18.8 7.2 Total % .2 2.0 .3 .0 .0 .0 .0 1.1 .0 2.6 .1 .6 .1 7.2 J N 120 1,913 225 103 14 1 29 1,732 27 5,011 245 828 64 1,0314 ICD % 1.2 18.5 2.2 1.0 .1 .0 .3 16.8 .3 48.6 2.4 8.0 .6 100.0 group % 7.1 9.6 7.0 5.8 4.0 12.5 24.2 16.1 2.8 26.8 13.1 9.8 11.1 11.5 Total % .1 2.1 .3 .1 .0 .0 .0 1.9 .0 5.6 .3 .9 .1 11.5 K N 85 877 68 37 2 2 12 493 6 7,035 32 323 116 9,089 ICD % .9 9.6 .7 .4 .0 .0 .1 5.4 .1 77.4 .4 3.6 1.3 100.0 group % 5.1 4.4 2.1 2.1 .6 25.0 10.0 4.6 .6 26.1 1.7 3.8 20.2 10.1 Total % .1 1.0 .1 .0 .0 .0 .0 .5 .0 7.9 .0 .4 .1 10.1 L N 7 153 24 24 15 0 0 91 2 297 9 50 7 679 ICD % 1.0 22.5 3.5 3.5 2.2 .0 .0 13.4 .3 43.8 1.3 7.4 1.0 100.0 group % .4 .8 .7 1.4 4.3 .0 .0 .8 .2 1.6 .5 .6 1.2 .8 Total % .0 .2 .0 .0 .0 .0 .0 .1 .0 .3 .0 .1 .0 .8 M N 607 7,685 1,030 1,247 101 3 6 1,493 689 4,635 252 3,404 31 21,183 ICD % 2.9 36.3 4.9 5.9 .5 .0 .0 7.0 3.3 21.9 1.2 16.1 .1 100.0 group % 36.2 38.6 32.0 70.5 29.2 37.5 5.0 13.9 71.5 27.8 13.5 40.4 5.4 23.6 Total % .7 8.6 1.1 1.4 .1 .0 .0 1.7 .8 5.2 .3 3.8 .0 23.6 N N 26 970 194 54 13 0 6 373 27 3,845 247 276 17 6,048
Group Total Pro re nata Name of the disease or symptoms Doctor’s name or instructions Drug name Emergency System error Inflammation No specific meaning Not to be taken orally Not to be taken at the same time Related to surgical operations Benefits exceed dangers Ambiguous reasoning ICD % .4 16.0 3.2 .9 .2 .0 .1 6.2 .4 63.6 4.1 4.6 .3 100.0 group % 1.5 4.9 6.0 3.1 3.8 .0 5.0 3.5 2.8 21.9 13.2 3.3 3.0 6.7 Total % .0 1.1 .2 .1 .0 .0 .0 .4 .0 4.3 .3 .3 .0 6.7 O N 1 30 24 0 0 0 0 21 8 345 1 6 1 437 ICD % .2 6.9 5.5 .0 .0 .0 .0 4.8 1.8 79 .2 1.4 .2 100.0 group % .1 .2 .7 .0 .0 .0 .0 .2 .8 1.3 .1 .1 .2 .5 Total % .0 .0 .0 .0 .0 .0 .0 .0 .0 .4 .0 .0 .0 .5 P N 3 47 1 1 0 0 1 111 0 54 0 16 2 236 ICD % 1.3 19.9 .4 .4 .0 .0 .4 47.0 .0 22.9 .0 6.8 .8 100.0 group % .2 .2 .0 .1 .0 .0 .8 1.0 .0 .2 .0 .2 .3 .3 Total % .0 .1 .0 .0 .0 .0 .0 .1 .0 .1 .0 .0 .0 .3 Q N 9 125 40 0 4 0 0 165 6 387 1 46 5 792 ICD % 1.1 15.8 5.1 .0 .5 .0 .0 20.8 .8 48.8 .1 5.8 .6 100.0 group % .5 .6 1.2 .0 1.2 .0 .0 1.5 .6 1.4 .1 .5 .9 .9 Total % .0 .1 .0 .0 .0 .0 .0 .2 .0 .4 .0 .1 .0 .9 R N 72 881 179 21 13 0 0 555 36 3,217 264 285 12 5,535 ICD % 1.3 15.9 3.2 .4 .2 .0 .0 10.0 .7 58.2 4.8 5.1 .2 100.0 group % 4.3 4.4 5.6 1.2 3.8 .0 .0 5.2 3.7 21.3 14.1 3.4 2.1 6.2 Total % .1 1.0 .2 .0 .0 .0 .0 .6 .0 3.6 .3 .3 .0 6.2 S N 30 987 403 32 48 0 14 905 23 3,955 279 708 10 7,395 ICD % .4 13.3 5.4 .4 .6 .0 .2 12.2 .3 53.4 3.8 9.6 .1 100.0 group % 1.8 5.0 12.5 1.8 13.9 .0 11.7 8.4 2.4 22 14.9 8.4 1.7 8.2 Total % .0 1.1 .4 .0 .1 .0 .0 1.0 .0 4.4 .3 .8 .0 8.2 T N 6 234 23 3 1 0 2 95 2 1,283 112 71 1 1,833 ICD % .3 12.8 1.3 .2 .1 .0 .1 5.2 .1 70 6.1 3.9 .1 100.0 group % .4 1.2 .7 .2 .3 .0 1.7 .9 .2 8.4 6.0 .8 .2 2.0 Total % .0 .3 .0 .0 .0 .0 .0 .1 .0 1.5 .1 .1 .0 2.0 U N 0 1 0 0 0 0 0 0 0 5 0 1 0 7 ICD % .0 14.3 .0 .0 .0 .0 .0 .0 .0 71.4 .0 14.3 .0 100.0